Différence entre la trypsine et la pepsine | Trypsine vs Pepsine
Différence - Trypsine vs Pepsine
Les enzymes digestives sont les enzymes qui brisent les aliments que nous consommons en petites molécules qui peuvent être absorbées par notre corps. Ces enzymes aident à l'absorption des nutriments et au maintien d'un intestin sain. Ils sont les chevaux de labour de notre système digestif et sont impliqués tout au long du processus digestif. Nous consommons divers types d'aliments composés de graisses, de protéines et de glucides. Différentes enzymes digestives travaillent ensemble et se cassent pour casser cette nourriture en composants plus petits et plus absorbables. Les enzymes digestives sont sécrétées par les glandes salivaires, les cellules sécrétrices de l'estomac et du pancréas et les glandes sécrétoires de l'intestin grêle. Il existe quatre catégories fondamentales d'enzymes digestives. Ce sont des protéases, des lipases, des amylases et des nucléases. Les protéases, également connues sous le nom de peptidases, cassent les protéines en peptides ou en acides aminés. La trypsine et la pepsine sont deux protéases.
La pepsine est la principale enzyme digestive de l'estomac. La trypsine est présente dans les sucs pancréatiques sécrétés dans l'intestin grêle. C'est la différence clé entre la trypsine et la pepsine.
TABLE DES MATIÈRES1. Vue d'ensemble et différence clé
2. Qu'est-ce que la trypsine
3. Qu'est-ce que Pepsin
4. Similitudes entre la trypsine et la pepsine
5. Comparaison côte à côte - Trypsine vs Pepsine sous forme tabulaire
6. Résumé
Qu'est-ce que la trypsine?
La trypsine est une protéase sécrétée par le pancréas dans l'intestin grêle. La trypsine digère les protéines en peptides et en acides aminés. La trypsine est formée sous la forme inactive connue sous le nom de trypsinogène. Le trypsinogène est activé dans la trypsine par une enzyme appelée enteropeptidase. La trypsine activée catalyse la séparation des protéines en acides aminés dans des conditions basiques.
Figure 01: Trypsine
La trypsine a été découverte pour la première fois par Wilhelm Kuhne en 1876. La trypsine rompt les chaînes peptidiques principalement du côté carboxyle des acides aminés lysine ou arginine. Il existe des inhibiteurs naturels de trypsine afin d'empêcher l'action de la trypsine active dans le pancréas, ce qui peut être très dommageable. Ce sont le pancréas bovin, l'ovomucoïde, le soja et le haricot de Lima. Ces inhibiteurs agissent comme des analogues de substrat compétitifs et empêchent la liaison du substrat correct dans le site actif de la trypsine. Lorsque ces inhibiteurs se lient à la trypsine, ils forment un complexe inactif.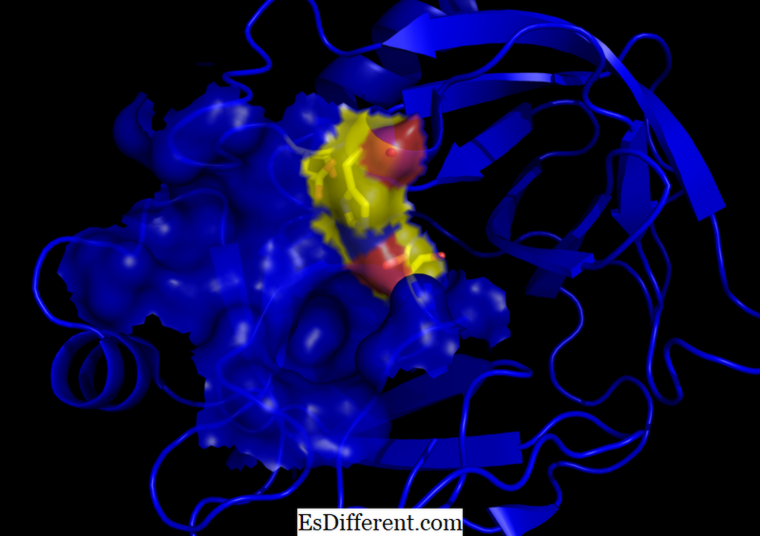
Qu'est-ce que la pepsine?
Différentes enzymes digestives sont incluses dans le suc gastrique. La pepsine est la principale enzyme gastrique parmi eux. Pepsin a été découvert par Theodor Schwann en 1836.La structure de Pepsin est tridimensionnelle. Le site actif de l'enzyme est formé en tordant et en repliant les chaînes polypeptidiques et en rapprochant plusieurs acides aminés l'un de l'autre. La pepsine est produite par les glandes gastriques de l'estomac. Il est formé sous la forme inactive connue sous le nom de pepsinogène et converti en la forme active, qui est la pepsine, par le HCl dans l'estomac. La pepsine est une protéase. Il décompose les protéines en peptides ou en acides aminés. L'estomac a des conditions acides. La catalyse à la pepsine se produit sous cet environnement acide de l'estomac.Figure 02: Pepsine
La pepsine est efficace pour briser les liaisons peptidiques entre les acides aminés hydrophobes et aromatiques tels que la phénylalanine, le tryptophane et la tyrosine. L'action de la pepsine peut être inhibée en créant des environnements fortement alcalins et des inhibiteurs tels que la pepstatine, le sucralfate, etc.

Quelles sont les similitudes entre la trypsine et la pepsine?
La pepsine et la trypsine décomposent les protéines. Les deux sont des proteases principales dans le système digestif humain.
Les deux enzymes sont sécrétées sous des formes inactives telles que le pepsinogène et le trypsinogène.
- Quelle est la différence entre la trypsine et la pepsine?
- - diff Article Milieu avant Tableau ->
Trypsine vs Pepsine
La trypsine est une protéase qui agit dans l'intestin grêle.
La pepsine est une protéase qui agit dans l'estomac. |
|
| Milieu | La trypsine agit en milieu alcalin |
| La pepsine agit en milieu acide. | |
| Localisation | La trypsine se trouve dans l'intestin grêle. |
| La pepsine se trouve dans l'estomac. | |
| Type de protéase | La trypsine est une protéase pancréatique. |
| La pepsine est une protéase gastrique. | |
| Forme inactive | La forme inactive de la trypsine est le trypsinogène. |
| La forme inactive de Pepsin est pepsinogène. | |
| Activation | Le trypsinogène est activé dans la trypsine par une enzyme appelée enteropeptidase. |
| Le pepsinogène est activé dans la pepsine par le HCl. | |
| Découverte | Trypsine a été découvert par Wilhelm Kuhne en 1876 |
| pepsine a été découverte par Theodor Schwann en 1836. | |
| Résumé - Trypsine vs pepsine | et la pepsine sont Trypsine deux protéases qui agissent sur des protéines et rupture vers le bas en peptides et en acides aminés. La trypsine est produite par le pancréas et sécrétée dans l'intestin grêle. La pepsine est produite par les glandes de l'estomac. C'est l'une des principales enzymes gastriques. C'est la différence entre la trypsine et la pepsine. |
Télécharger la version PDF de Trypsine vs Pepsin
Vous pouvez télécharger la version PDF de cet article et l'utiliser pour des objectifs hors ligne selon la note de citation. S'il vous plaît télécharger la version PDF ici Différence entre la trypsine et la pepsine.
Références:
1. Peluso, Ph.D. Michael R. "Quelles sont les fonctions de la trypsine? "LIVESTRONG. COM. Leaf Group, 18 juin 2015. Web. Disponible ici. 21 juillet 2017.
2. "Pepsine. " Wikipédia. Fondation Wikimedia, 13 juillet 2017. Web. Disponible ici. 21 juillet 2017.
Courtoisie d'image:
1. "Site actif de la trypsine" Par Fdardel - Propre travail (CC BY-SA 3. 0) via Commons Wikimedia




