Différence entre Hydrophile et Hydrophobe Différence entre
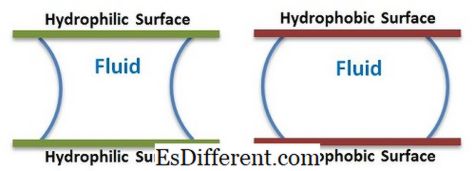
Hydrophile vs. Hydrophobe
Solvants, mélanges, composés et particules ne sont que quelques-uns des composants de la vie d'un chimiste. Les études impliquant l'observance du comportement des molécules dans un état ou un environnement donné peuvent sembler être l'un des travaux les plus effrayants pour ceux qui ont peu de connaissances en chimie et sciences connexes, mais ils sont très utiles pour présenter les derniers produits et développements dans diverses industries.
Les chimistes, les biologistes et les autres personnes qui poursuivent une carrière dans le domaine des sciences commencent leur carrière en obtenant la formation nécessaire dans les universités et les collèges. Quand ils décident d'avoir une carrière liée à la biochimie, leur éducation commence par des leçons qui leur permettent de mieux comprendre les activités et les comportements moléculaires.
Cela dit, il est sûr de supposer que les cours de base offerts au cours de leur première année de collège comprennent une évaluation de la nature hydrophobe et hydrophile des molécules et autres particules.
Le mot "hydro-" signifie "eau". "Ainsi, l'étude des molécules hydrophobes et hydrophiles concerne la solubilité et d'autres propriétés des particules lors de leur interaction avec l'eau. Le terme «phobique», qui provient de «phobie», se traduirait par «craintif de (l'eau)». "Les molécules et les particules hydrophobes, par conséquent, peuvent être définies comme celles qui ne se mélangent pas avec l'eau - elles le repoussent. D'un autre côté, les molécules hydrophiles sont celles qui interagissent bien avec H2O.
En d'autres termes, la distinction entre les molécules hydrophobes et hydrophiles est tirée par l'observation de la répulsion des particules hydrophobes de l'eau et de l'attraction des molécules hydrophiles vers l'eau.Dans une expérience de laboratoire, par exemple, on peut observer qu'il y a des solubles particuliers qui se dissolvent dans l'eau et d'autres qui ne le sont pas. Maquillage broyé et en poudre, par exemple, peut être capable de se dissoudre dans un verre plein d'huile de cuisson, mais pas dans un verre plein d'eau. D'autre part, le sel est facilement absorbé par l'eau, mais il ne se dissout pas dans l'huile.
Le maquillage broyé et pulvérisé peut donc être vu comme des particules hydrophobes. Pendant ce temps, les étudiants peuvent arriver à la conclusion que les molécules de sel sont hydrophiles. Le sel peut conserver une forte affinité dans l'eau, qui peut l'absorber et le dissoudre. D'autre part, le maquillage à base d'huile contient des molécules qui repoussent et refusent de se combiner avec les molécules d'eau.
Mis à part les expériences en laboratoire, ce comportement moléculaire en référence à la nature hydrophobe et hydrophile est également observé lorsque les biologistes se penchent sur la perméabilité des membranes cellulaires.Notez que plusieurs particules peuvent entrer et sortir de la cellule à travers la membrane, qui est faite de bicouches lipidiques et de protéines.
Lorsque les particules sont hydrophobes, il se produit une simple diffusion passive, ce qui signifie que la molécule n'a pas besoin d'énergie pour entrer ou sortir de la cellule. C'est parce que la membrane cellulaire est livré avec des composants hydrophobes qui correspondent aux molécules.
D'autre part, les particules hydrophiles peuvent avoir besoin de supports protéiques pour faciliter la diffusion. C'est parce que les composants des molécules rejettent ceux de la membrane cellulaire.
Pour mieux comprendre cela, imaginez un verre d'eau et un verre d'huile de cuisson. Lorsque de l'eau est ajoutée à l'huile, il y a répulsion entre les molécules. Mais quand on met de l'eau dans l'eau et de l'huile dans l'huile, aucune réaction ne sera observée.
La chimie organique fournit une explication à ce phénomène. Notez que l'eau contient des molécules polaires; il s'ensuit donc que les substances polaires et les particules sont absorbées ou attirées par H2O. Les molécules hydrophiles sont connues pour être polaires et ioniques - elles ont des charges positives et négatives, qui peuvent attirer les molécules d'eau. Inversement, les particules hydrophobes sont connues pour être non polaires.
Résumé:
1. Hydrophile signifie aimer l'eau; des moyens hydrophobes résistants à l'eau.
2. Les molécules hydrophiles sont absorbées ou dissoutes dans l'eau, alors que les molécules hydrophobes ne se dissolvent que dans les substances à base d'huile.
3. Les molécules hydrophiles nécessitent une diffusion facilitée, tandis que les molécules hydrophobes conviennent à la diffusion passive dans les activités cellulaires.
4. Les molécules hydrophiles sont polaires et ioniques; les molécules hydrophobes sont non polaires.



